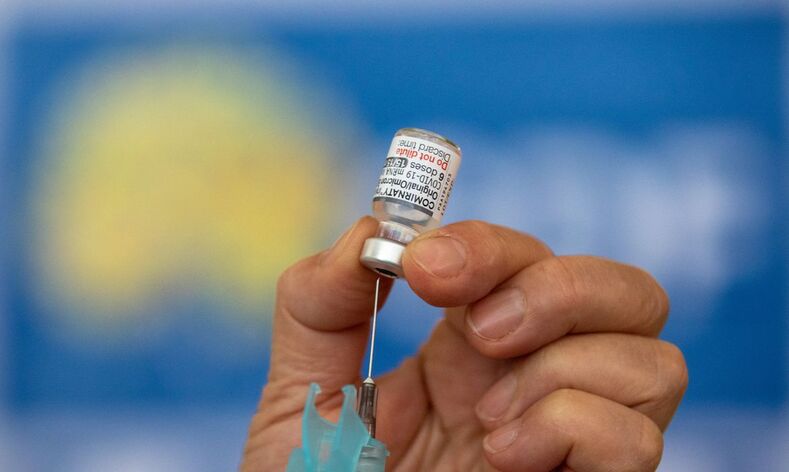
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, neste domingo (17), durante reunião extraordinária, os pedidos de uso emergencial das vacinas Coronavac e AstraZeneca, contra a Covid-19. O primeiro imunizante é desenvolvido pelo Instituto Butantan com o laboratório chinês Sinovac e já tem 6 milhões de doses prontas. A segunda vacina é da Universidade de Oxford.
Na apresentação, gerente de Medicamentos da Anvisa, Gustavo Mendes, informou que a área técnica confirmou a eficácia da CoronaVac. A taxa de sucesso na prevenção da doença em relação ao grupo que tomou placebo (medicamento inócuo) atingiu 50,39%. Na semana passada, o Butantan tinha divulgado uma eficácia de 50,38%. O índice está acima da eficácia mínima de 50% exigida pela Anvisa e recomendada pela Organização Mundial de Saúde (OMS).
“A recomendação como área técnica é que, tendo em vista o cenário da pandemia, o aumento do número de casos, a ausência de alternativas terapêuticas, que é uma situação de muita tensão quanto aos insumos, a agência recomenda a aprovação do uso emergencial, condicionada ao monitoramento e acompanhamento próximo das incertezas” , disse Mendes.
ASTRAZENECA
A outra vacina aprovada neste domingo foi a AstraZeneca, que é desenvolvida em parceria da Universidade de Oxford com a Fundação Oswaldo Cruz (Fiocruz). Neste primeiro lote, são dois milhões de doses produzidos na Índia. O envio para o Brasil depende do governo daquele país.
A Anvisa confirmou a eficácia global do imunizante em 70,42%, validando estudo publicado no início de dezembro pela revista científica The Lancet. A eficácia mede a taxa de sucesso na prevenção da covid-19 comparada a quem recebeu placebo (medicamento inócuo).